细胞壁合成相关抗真菌药物靶点的分子机制和药物作用机理研究
主要完成人:于洪军、张敏、胡鑫霖、杨坪、杨依争

侵袭性真菌感染临床多发于免疫缺陷、器官移植等高危人群,每年造成150多万人死亡,已成为全球关切的公共卫生问题,但是其治疗却面临药物种类有限、副作用大、耐药等严峻问题,因而对新药的需求非常迫切。真菌细胞壁合成途径是开发广谱、低毒抗真菌药物的关键靶点,对其分子机制和药物作用机理缺乏了解是阻碍相关药物开发优化的瓶颈。为解决这些难题,于洪军、张敏团队在华中科技大学基础医学院、细胞架构研究中心、人畜共患传染病重症诊治全国重点实验室以及国家科研项目的支持下,针对真菌细胞壁合成相关药物靶点开展了系统研究,取得了以下原创突出成果:
一是解析了真菌细胞壁葡聚糖合成的分子基础和一线抗真菌药物棘白菌素的耐药机制。
β-1,3-葡聚糖是真菌细胞壁核心成分,其靶向药物包括棘白菌素等临床一线药物,但是β-1,3-葡聚糖合成酶仍需确认,其功能机制、药物作用和耐药机理也不清楚,严重限制了相关药物开发。研究团队设计并筛选到影响FKS1活性的重要突变(S643P),克服了FKS1的易失活难题,首次直接证明了FKS1可以特异性合成β-1,3-葡聚糖,解决了领域内的关键问题(图1)。团队进一步开发了针对FKS1的药物筛选新方法,无需放射性标记,为创新药物的大规模筛选开发奠定了重要基础。团队接着鉴定出药靶FKS1的催化反应中心和产物转运通道两大功能区域,并通过系统性突变以及体内、体外功能分析,深入揭示了FKS1合成β-1,3-葡聚糖的分子机制,为抗真菌药物的设计开发提供了关键的干预位点和理论基础(图2)。在探索棘白菌素药物作用机制的过程中,团队发现了耐药突变集中分布于富含有序lipid的区域,形成潜在药物结合位点;相关药物作用测试证实了这些位点的突变会显著降低FKS1对药物的敏感性;团队还发现耐药突变引发了耐药热点区域的显著构象变化以及附近脂分子重排,揭示了耐药性产生的独特分子机理,为认识和解决临床耐药问题提供了重要启示和依据(图3)。
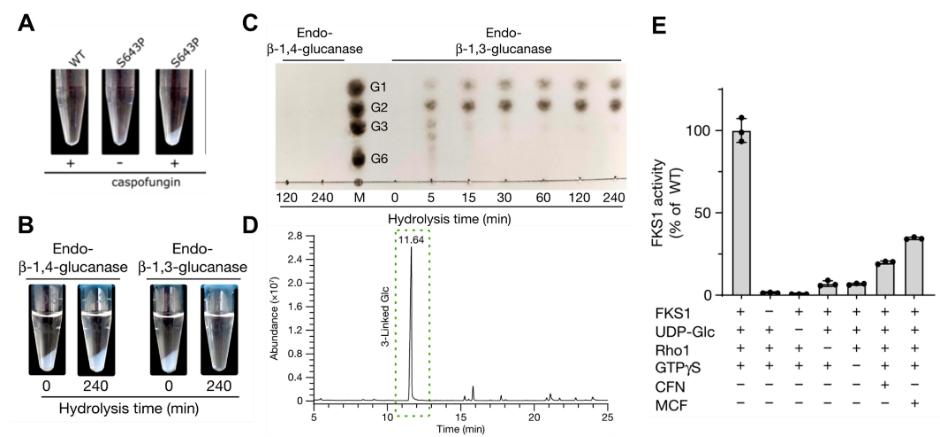
图1 β-1,3-葡聚糖合成酶的确认及FKS1药物筛选体系的建立
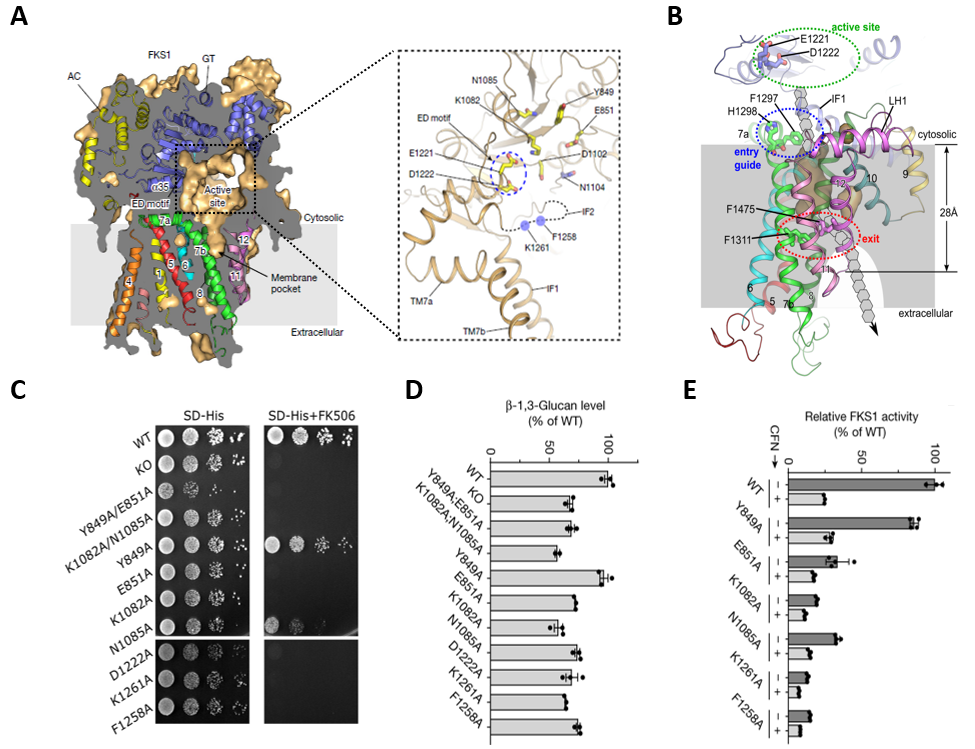
图2 药物靶点FKS1合成β-1,3-葡聚糖的分子机制解析
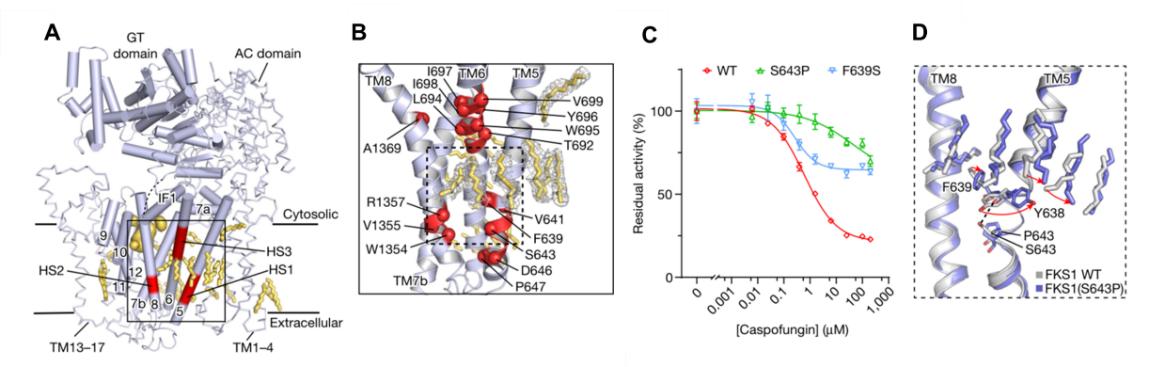
图3 FKS1临床耐药突变的空间分布规律以及耐药性产生机制分析
二是阐明了真菌细胞壁几丁质合成机理和抗真菌药物Nikkomycin Z作用机制。
几丁质是多种致病真菌细胞壁的重要成分,由几丁质合成酶催化合成,其靶向药物Nikkomycin Z已被应用在真菌感染的临床治疗研究中,然而几丁质合成酶的分子机制以及药物抑制机理尚不清楚。研究团队系统表征了几丁质合成酶Chs1的酶活特征和药物作用特点,并通过分析Chs1、Chs1与药物复合物的多个高分辨率结构,阐明了Chs1合成和跨膜转运几丁质的关键分子机制,揭示了Nikkomycin Z与Chs1形成的特异性相互作用,阐明了药物的竞争性抑制作用原理,为靶向几丁质合成的药物开发优化提供了分子水平的理论基础(图4)。
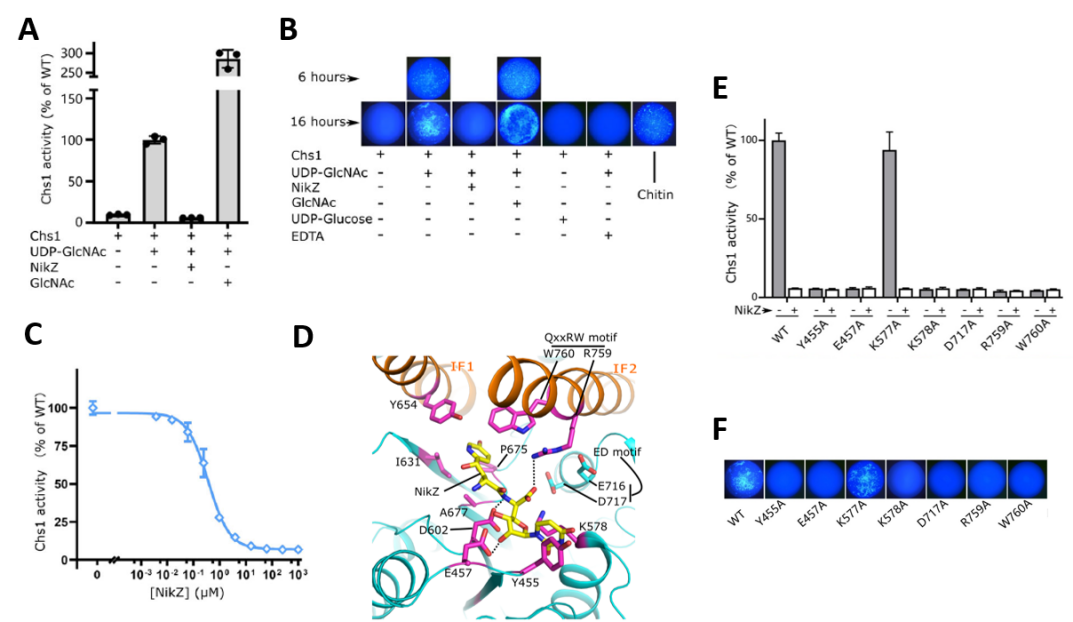
图4 几丁质合成酶Chs1的分子机制研究以及抗真菌药物Nikkomycin Z的作用机理解析
上述系列研究成果相继发表在国际知名期刊Nature、CellDiscovery,是抗真菌药物靶点研究领域的重要进展,对于相关药物开发优化、解决侵袭性真菌感染等重大问题具有重要的学术和应用价值,因而迅速获得了国内外的广泛关注,被知名期刊、真菌研究领域知名专家等报道和高度评价:Nature Chemical Biology发表的题为“Fungal FKS in focus”的专门评述认为该工作“为新型抗真菌化合物的设计铺平了道路”;抗真菌药物公司Bright Angel Therapeutics联合创始人、加拿大多伦多大学副校长Leah Cowen教授高度肯定了该成果 “为靶向这一重要抗真菌靶点来开发更有效的药物提供了平台”;美国Hackensack Meridian Health发现与创新研究中心首席科学家与执行副主席David Perlin教授强调该工作“为认识棘白菌素药物的结合位点提供了见解,并深入了对FKS1特定位点产生耐药性的理解”。