新闻网讯 12月12日,基础医学院宇兴江教授课题组在Advanced Science上发表了题为“Transgelin促进胶质瘤干细胞的低氧应答反应并通过调控p53的乙酰化水平维持干细胞的稳定性”(Transgelin promotes glioblastoma stem cell hypoxic responses and maintenance through regulation of p53 acetylation)的研究论文,阐释了低氧微环境下促癌基因TAGLN如何促进GSC的自我更新以及TAGLN/HDAC2的靶向药-丙戊酸钠(Sodium valproate,VPA)与天然冰片联用对荷瘤小鼠生存的影响。

多形性胶质母细胞瘤(Glioblastoma multiforme, GBM) 是颅内最常见的恶性程度最高的原发性肿瘤,虽然经过治疗但5年生存率仍基本不变。随着单细胞测序等技术的应用,越来越多的GBM中异常基因被筛选出来。因此,有必要寻找多形性胶质母细胞瘤的致病基因、并对其致病机制及其转化应用进行深入探讨。
GSC是一群具有无限自我更新能力、不断增殖潜能、各谱系分化能力和体内肿瘤重建能力的细胞类群,因此GSC是GBM中的治疗关键。GSC多处于低氧微环境中,低氧不仅可以导致肿瘤内异质性的产生,也是胶质瘤难治的主要原因之一。了解低氧微环境下维持GSC稳定性的信号转导途径对开发新型难治性神经系统肿瘤的药物至关重要。
2022年,宇兴江课题组发现低氧下,受HIF1α调控的关键基因-HMGB1可以分泌到GSC的胞外,通过自分泌或旁分泌的方式与GSC膜上的RAGE受体结合,促进ERK的磷酸化入核后激活下游细胞周期关键蛋白,促进了GSC的自我更新。
TAGLN (Transgelin) 首次在鸡胃平滑肌上发现的一种丰富的22-kDa蛋白(SM22),是钙调蛋白家族的成员。越来越多的研究发现TAGLN在肿瘤组织中的表达差异,包括GBM。研究人员主要探索TAGLN在GBM中的表达情况及其与GBM和GSC的病理生物学特征的联系。研究在低氧环境下,GSC中TAGLN的表达水平及调控机制。在低氧微环境下,研究TAGLN对GSC的功能影响以及作用机制。寻找靶向TAGLN的特异性药物,并检验其在体内和体外的治疗效果,为药物推广至临床提供理论基础。
研究人员发现TAGLN是多形性胶质母细胞瘤发生发展过程中重要的促癌基因并可作为GSC的生物学指示物。低氧可以诱导TAGLN在GSC中特异性高表达。低氧微环境下,TAGLN作为低氧转录调节因子调控HIF1α的表达水平。
除此之外,研究人员还发现,低氧下TAGLN可以促进GSC的自我更新,而敲低TAGLN可延长荷瘤小鼠的存活时间。低氧微环境中,TAGLN与HDAC2形成蛋白复合体通过增强p53的去乙酰化水平,促进下游细胞周期关键蛋白的表达,从而促进GSC不断地自我更新。血脑屏障通透剂-天然冰片联合TAGLN/HDAC2的特异性抑制剂-VPA治疗荷瘤小鼠后可以延长小鼠的存活时间。
综上所述,这项研究首次发现了低氧下TAGLN在GSC中具有转录调节因子的功能,通过与HIF1α相互作用形成低氧转录复合体,维持低氧下GSC的稳定性。另外,研究人员详细阐述了低氧下TAGLN促进低氧下GSC的自我更新的机制。研究人员的中西药联合应用的新型给药方式将为临床GBM患者提供新的治疗方法。
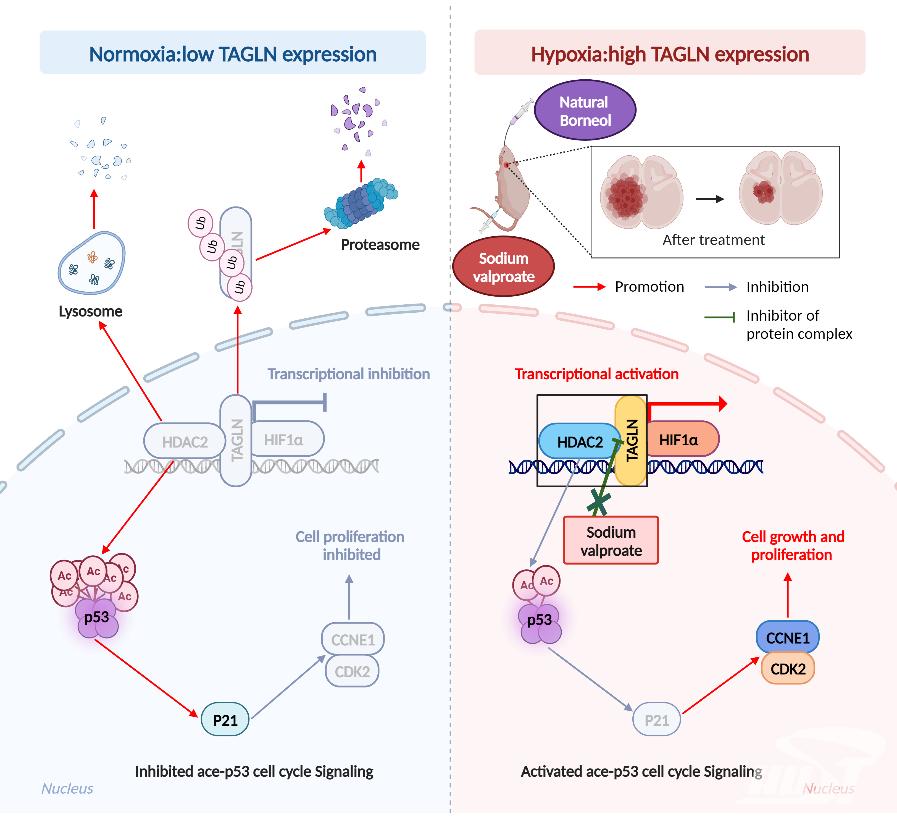
低氧下,在GSC中高表达的TAGLN促进GSC自我更新及常氧下GSC自我更新被抑制的作用机制模式图。
基础医学院博士生李环是这项研究的第一作者,课题组宇兴江教授和美国匹兹堡大学Jeremy N. Rich教授为本研究的共同通讯作者。该研究工作得到了国家自然科学基金、华中科技大学学术前沿青年队项目以及华中科技大学自主创新基金的支持。